使用二氧化氯控制THMs
Control of THMs with Chlorine Dioxide
John Newlove Jennifer Miller, Ph.D.Greg D. Simpson, Ph.D.
(Vulcan Performance Chemicals)
张东署 译
Abstract Chlorine dioxide (ClO2) is effective as both a disinfectant and an oxidant in potable water and wastewater treatment. Its selective reactivity makes chlorine dioxide a powerful oxidizing agent useful in many water treating applications for which chlorine and other oxidizing agents are unsuitable. Unlike chlorine, chlorine dioxide does not react with naturally occurring organic materials to form trihalomethanes (THMs). Chlorine dioxide aids in reducing the formation of Total Trihalomethanes (TTHMs) and haloacetic acids (HAA) by oxidizing THM precursors.
The US EPA’s National Primary Drinking Water Regulations1 set a maximum contaminant level (MCL) of 0.08 mg/L for TTHM.The EPA has identified chlorine dioxide as an alternative or supplemental oxidant-disinfectant that is one of the most suitable for TTHM treatment and control2.
This paper provides a brief overview of THM formation and the use of chlorine dioxide for preventing or controlling THMs. Two case histories are presented.
Keyword Chlorine Dioxide THMs Control
摘要 饮用水和废水处理中,二氧化氯是一种有效的消毒剂和氧化剂。其选择性反应特性可以使其作为一种强氧化剂,在氯和其它氧化剂不适用的情况发挥作用。而且与氯不同的是,二氧化氯不会与水中天然存在的一些有机物质发生反应生成三卤甲烷(THMs)。并且二氧化氯可以通过氧化THMs的母体有机物。从而减少TTHMs(水中总三卤甲烷量)及HAA(卤代乙酸)的产生。美国环保总署对于饮用水中TTHMs最大浓度标准为0.08mg/l[1],并且认定在需要对TTHMs进行控制和处理的情况下,二氧化氯可以作为一种替代或补充氧化消毒剂而使用[2]。本文简要概述了THMs的生产原理及使用二氧化氯控制或减少THMs,并对以往的文献进行了总结。
关键词 二氧化氯 三卤甲烷
1. 简介
估计美国有1200万人使用的饮用水是由亚氯酸钠制备出来的二氧化氯消毒的。二氧化氯不但能高度有效地控制饮用水中的水生病原体,而且很少生成卤化消毒副产物。二氧化氯是一种广谱杀菌剂,和氯气一样,能有效地灭杀病毒、细菌和真菌,二氧化氯对孢子寄生虫如Giardia和Cryptosporidium灭杀效果要比氯气好。另外,二氧化氯也能够有效地去除嗅、味、色、铁和锰。
1.1 二氧化氯的消毒作用
美国国家基本饮用水管理条例规定[3],饮用水的消毒处理必须确保至少99.9%(3-log)的Giardia lamblia孢子被去除并且/或者灭活;而肠道病毒的去除率并且/或者灭活率至少要达到99.99%(4-log)。只要具备必要的CT值,二氧化氯灭活99.9%的Giardia lamblia孢子和99.99%的肠道病毒是有保证的。此外,美国环保总署最近发布的Stage 2关于微生物和消毒副产物联邦顾问委员会协议[4]中指出使用二氧化氯来控制Cryptosporidium是一种可以接受的方案。
二氧化氯和氯气一样能够有效地阻止废水中大肠杆菌的繁殖,而且它对二级出水中病毒的灭杀效果比氯气好[5]。
1.2 二氧化氯对三卤甲烷的(THM)控制
二氧化氯与三卤甲烷的前体腐殖质反应不会生成THMs。在预处理阶段用二氧化氯氧化THM的前体,然后氯气作为消毒剂在凝结、沉淀和过滤后加入。这样处理后的饮用水比常规氯气处理所产生的THMs少50-70%。
1.3 二氧化氯对味和嗅的去除
二氧化氯的浓度达到1mg/L时,就能够有效去除藻类和植物腐烂所产生的味和嗅,二氧化氯能够氧化低阈值的有异味的化合物,这些化合物包括:二甲萘烷醇,2,3,6-三氯茴香醚(TCA), 2-甲基异冰片(MIB)以及吡嗪类化合物。二氧化氯还能有效去除产生异味的酚类化合物,在此处理过程中,很少产生氯酚[6]。已有试验证明对于硫醇和有机二硫化合物这类有异味的物质,同样可以用二氧化氯来氧化去除[7]。
1.4 二氧化氯对铁和锰的去除
在美国,大约有40%的生活用水中铁和锰的含量超过推荐的中级最大允许浓度。根据推荐的浓度指标,铁含量不超过0.3mg/L ,锰含量不超过0.05 mg/L 。之所以这样规定是因为铁和锰等于或超过此含量会使水有颜色、浑浊、着色以及口感不佳。铁和锰也可能会加速分散系统中微生物的生长,进一步恶化水的味、嗅以及色的情况。二氧化氯能快速与溶解于水中铁和锰反应生成不溶于水的沉淀物,然后可以用沉淀和过滤的方法将沉淀物从水中分离出去。用二氧化氯预氧化铁和锰同样能提高其的沉积效果,产生更好的滤出时间[8]。
2. 三卤甲烷的形式
70年代后期,研究人员指出饮用氯气处理后的水可能会提高患癌症的几率[9][10],潜在的致癌物质就是三卤甲烷(THMs[11][12])。美国环保总署规定,饮用水中THM的含量不得超过0.1 mg/L 。通过对减少饮用水中三卤甲烷方法的探讨[1][13-15],环保总署在1983提出二氧化氯可以作为控制THMs有效的手段。
更多研究表明:地面水特别是当水中腐殖酸和灰黄霉酸的含量很高时用氯气处理后,三卤甲烷的含量会显著提高。过去由于检测手段的限制,无法对水中不同成分逐一检测,因此把它们作为三卤甲烷总量来测定。随着检测手段的提高,现在已经可以对不同的三卤甲烷进行检测。用氯气对饮用水进行处理后,会在水中生成致癌物质,如氯仿、溴二氯甲烷以及其它消毒副产物(DBPs)。
注1: MCLG 表示最大允许浓度期望值
最终的消毒剂及消毒副产物条例(DBPR)规定,饮用水中三卤甲烷总量的最大允许浓度(MCL)为0.08 mg/L ,并且将此规定延伸至所有相似的水体。此外,最近规定卤代乙酸的最大允许浓度为0.06 mg/L,目前对各组分的限定范围见表1。
3.二氧化氯对三卤甲烷的处理
与氯气相反,二氧化氯和腐殖质(三卤甲烷的前体)反应不会生成THMs,尽管在二氧化氯处理后的水中可以检测到微量的三卤甲烷,这是由于二氧化氯中所含的痕量氯气杂质所致。
1976年,Miltner 证明用二氧化氯对饮用水进行消毒只产生极微量的三卤甲烷[16]。后来在Evansville, Indiana[17]; Hamilton, Ohio[18];Galveston, Texas[19]; Louisville, Kentucky[20]; Davenport Iowa[21]; 和Contra Costa, California[14]等地的现场试验得到了和Miltner相同的结论。
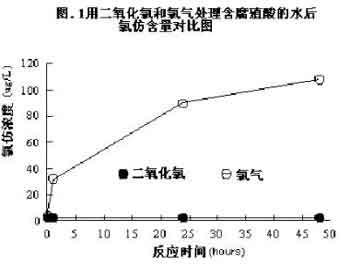
此外,Noack 和Doerr 在1978年作了关于氯气、二氧化氯以及氯气和二氧化氯结合起来氧化饮用水中腐殖酸的报道[22]。报道中指出,在二氧化氯浓度不高的情况下,它与水中腐殖酸的反应速率要远远小于它在浓度较高时的反应速率,正如所预料的是与氯气不同,二氧化氯与腐殖酸反应不会产生氯仿。试验结果如图1所示。
1984年,Rav-Acha 发现许多前期关于二氧化氯产生氯化有机物(包括三卤甲烷)的研究工作过高地估计了二氧化氯在正常投加浓度下所产生氯化有机物的量[15]。他报道在通常的二氧化氯使用条件下处理后的饮用水中检测不到THMs,这与Miltner[16], Henderson等人[23], 和Miller等人[13]的试验结果吻合。他指出二氧化氯消毒所产生的主要是氧化副产物而不是氯化副产物。他同样注意到二氧化氯与氯气相比,在天然水中选择性更高而且相对氯气而言,二氧化氯投加浓度一定。
Lykins在1986年报道,用二氧化氯预处理可以减少饮用水中三卤甲烷的含量[24]。在二氧化氯预处理以前,三卤甲烷的总含量是141 μg/L ,处理后总含量降至1.4 μg/L 。二氧化氯处理后的水用GC-MS分析,未检测到氯化副产物。在其它水处理厂也得到了同样的结果[25]。
ndrews[26]最近在加拿大使用二氧化氯进行消毒实验, 结果表明用氯气消毒后TTHMs为30 μg/L,而二氧化氯处理后TTHMs为5μg/L以下,用二氧化氯处理后,卤代乙酸(HAA’s)由氯气消毒后的20μg/L以上降为8μg/L以下;此外,对Giardia的灭杀率也从90%以下提高到99.9%。这说明在水中残余的二氧化氯仍然具有很好的消毒效果。
总而言之,二氧化氯消毒机理为氧化反应[27][28]。氯气除了氧化反应以外,还有很大一部分发生了副反应[23],其结果就是产生了卤代有机物,如三卤甲烷。人们研究了很多方法来去除由于氯气消毒所产生的三卤甲烷,二氧化氯是一种行之有效的方法,能够从本质上减少三卤甲烷的形成。
3.1 二氧化氯投加量
二氧化氯一般在原水中的投加浓度范围为0.1到5.0 mg/L。对大多数城市用水以及其它饮用水系统而言,为了保证消毒效果,需要二氧化氯在水中的余量达到2.0mg/L。处理后的水中也可以投加二氧化氯来保持消毒剂一定的残留量。二氧化氯投加的量与水本身的状况、污染程度以及处理级别有关系。美国饮用水基本管理条例和州饮用水标准规定,必须对水中残余的消毒剂和消毒副产物进行监测。对于工业废水和生活污水的处理而言,要保证其处理效果,一般认为二氧化氯的残余量应达到5mg/L。
3.2 二氧化氯投加方法
二氧化氯是由亚氯酸钠和一种氧化剂或者一种酸性介质反应制备出来的气体物质。通过二氧化氯发生器将亚氯酸钠转化为二氧化氯,然后稀释成二氧化氯溶液后使用。应该在处理系统中选择一个适当的地点投加二氧化氯,这是为了使加入的二氧化氯可以得到充分的混合并且在系统中均匀的分布。投加药剂的地点应该位于水位线以下,这可以防止二氧化氯挥发。不要把亚氯酸钠直接投加到饮用水中。
3.3 二氧化氯的分析
消毒副产物管理条例(DBPR)规定:除了对消毒副产物监测以外,对二氧化氯作消毒剂或氧化剂的饮用水系统中所含的二氧化氯以及亚氯酸根也要进行监测。尽管这些规定和方法未必适用于其它国家,但在美国这些规定是完整的。
二氧化氯:在美国,监测二氧化氯的余量建议采用下列两种方法(详见《水和废水标准测试方法》第20版)之一:
DPD 法,4500-ClO2 D
电流滴定法II,4500-ClO2 E[29]
上述方法是政府部门推荐的监测方法,还可以采用DPD比色法测试装置来测量系统中消毒剂二氧化氯的余量。
亚氯酸钠:对于水中亚氯酸根的监测而言,必须采用下面所推荐的三种方法(详见《水和废水标准测试方法》第20版)之一:
电流滴定法II,4500-ClO2 E
离子色谱法,EPA法300.0[30]
离子色谱法,EPA 法300.1[31]
特别规定电流滴定法可以用于对加药点亚氯酸根浓度的日常监测,但是对于系统内部亚氯酸根每月的或者附加的监测必须采用离子色谱法。
4.应用实例
4.1 实例1:二氧化氯对嗅和味的去除及其对三卤甲烷的控制
美国某大城市,每天消毒处理的饮用水量为1200万-3600万加仑。水中富含100多种有嗅和味的物质,水厂为此感到很头痛。过去对进入水厂原水进行处理的消毒剂主要是氯气,结果消毒后的水中THMs 含量相当高,因此需要找到一种消毒剂来取代氯气,要求该消毒剂不但能够有效地去除水的嗅和味、抑制THM的产生,而且具有足够的消毒效果。
有人建议市政当局用二氧化氯来处理原水,采用Rio LindaÒ公司生产的双组分流动发生器(加料速度为1.75-2.0 mg/L)对原水进行处理,结果证明二氧化氯的效果确实很好。
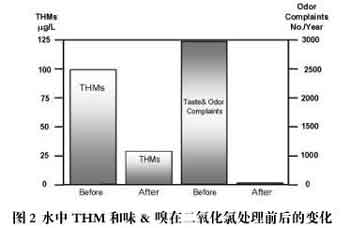
原水经过二氧化氯处理后,嗅和味明显地减少了,同时饮用水中THMs的含量甚至下降到美国环保总署规定的指标以下。另外,二氧化氯在水厂中使用结果显示它的消毒性能也很好。二氧化氯从1998年开始作为饮用水消毒剂,而且公众对它消毒效果非常满意。图2表示饮用水用二氧化氯处理前后的嗅和味及三卤甲烷的变化。
4.2 实例2:使用二氧化氯控制城市饮用水中的THMs
在美国东南部某市,每天有3300万加仑的饮用水经过消毒处理,过去对进入水厂原水进行处理的消毒剂主要是氯气,结果消毒后的饮用水中THMs 含量相当高,因此需要找到一种消毒剂来取代氯气,要求该消毒剂不但具有足够的消毒效果,而且能够有效地抑制THM的产生。
有人建议市政当局用二氧化氯来处理原水,采用Rio LindaÒ公司生产的双组分流动发生器(加料速度为0.5mg/L)对原水进行处理,还有人建议氯气可作为消毒剂在后续阶段使用。
二氧化氯能够有效降低饮用水中THMs的含量,甚至可以使其降低到美国环保总署规定的指标以下。运用二氧化氯处理的其他好处是:控制铁和锰的含量;在消毒的同时能氧化有异味的物质。二氧化氯从1992年开始作为饮用水消毒剂,而且公众对它消毒效果非常满意。图3表示饮用水用二氧化氯处理前后三卤甲烷含量的变化。

4.3 结论
在饮用水处理中,二氧化氯已被确证为一种有效的抑制或减少THMs生成的方法。此外,二氧化氯用在饮用水的前处理和后处理阶段,能够有效控制水的味和嗅以及去除水中的铁和锰。
作为氯气的替代品,二氧化氯不仅经济而且有效。因此,美国环保总署已把二氧化氯列为可替代或补充的用于处理和控制TTHM的最佳氧化—消毒剂之一[2]。
参考文献
1. Federal Register, National Primary Drinking Water Regulations: Disinfectants and Disinfection Byproducts, 63 FR 69389 (December 16, 1998).
2. USEPA, “Alternative Disinfectants and Oxidants Guidance Manual “EPA/815/R-99/014, (April 1999).
3. Code of Federal Regulations, National Primary Drinking Water Regulations, Subpart H – Filtration and Disinfection. 40 CFR 141.70-.75.
4. Federal Register, Stage 2 Microbial and Disinfection Byproducts Federal Advisory Committee Agreement in Principal(Stage 2 M-DBP Agreement), 65FR83015, (December 29, 2000).
5. Roberts, P.V., Aieta, E.M., Berg, J.D., and Chow. B.M., “Chlorine Dioxide for Wastewater Disinfection: A Feasibility Evaluation,” Stanford University, EPA-600/2-81-092 (1981).
6. Lalezary, S., Pirbdzdri, M., Mc.Guire, M.J., “Oxidation of Five Earthy-Musty Taste and Odor Compounds”, JAWWA, 62-69, (March 1986).
7. Warf, C.C. Jr., “Chlorine Dioxide and The Small Drinking Water System”, published in Providing Safe Drinking Water in Small Drinking Water Systems, Lewis Publishers, 121-131 (1998).
8. Stevens, A.A., “Reaction of Chlorine Dioxide”, Environ. Health Perspect., 46;101 (1982)
9. Alavanja, M., Goldstein I., and Sasser, M., "A Case Control Study of Gastrointestinal and Urinary Tract Cancer Mortality and Drinking Water Chlorination, in Water Chlorination,” in Environmental Impact and Health Effects, (edited by Jolley, R. L.), Vol. 2, pp. 395. Ann Arbor Science, Ann Arbor, MI., 1980.
10. Page, T., Harris, R. H., and Epstein, S. S., "Drinking Water and Cancer Mortality in Louisiana," Science 193, 55 (1976).
11. Report of the Carcinogenesis Bioassay of Chloroform. NTIS PB264018/AS, National Cancer Institute, 1976.
12. Roe, F. J. C., "Preliminary Report of Long-Term Tests of Chloroform in Rats, Mice and Dogs," unpublished Report. Cited in Ozone, Chlorine Dioxide and Chloramines as alternatives to Chlorine for Disinfection of Drinking Water. Water Supply Research, Office of Research and Development, U.S. EPA, Cincinnati, OH, 1976.
13. Miller, G. W., Rice, R. G., Robson, C. M., Kuhn, W., and Wolf, H., "An Assessment of Ozone and Chlorine Dioxide Technologies for Treatment of Municipal Water Supplies," EPA Report 600012-78-147, Cincinnati, OH, 1978.
14. Lange, A., and E. Kawczynski, 1978, "Controlling Organics, the Contra Costa County Water District," JAWWA 70:653.
15. Rav-Acha, Ch., 1984, “The Reactions of Chlorine Dioxide with Aquatic Organic Materials and Their Health Effects,” Water Res., 18(11):84.
16. Miltner, R. J., 1976, "The Effect of Chlorine Dioxide on Trihalomethanes in Drinking Water," MS Thesis, University of Cincinnati.
17. Lykins, B.W., Jr. and Griese, M.H., "Using Chlorine Dioxide for Trihalomethane Control," JAWWA, 78, 88 (1986).
18. Augenstein, H.W., "Use of Chlorine Dioxide to Disinfect Water Supplies," JAWWA, 66, 716 (1974).
19. Myers, G.L., et al., "Control of Trihalomethanes and Taste and Odor at Galveston County Water Authority," Proc. Annual Meeting, AWWA, at Denver, CO, 1667-1675 (1986).
20. Hubbs, S. A., M. Guers, and J. Siria, 1980, "Plant-scale Examination and Control of a ClO2-Chloramination Process at the Louisville Water Company," in Water Chlorination: Environmental Impact and Health Effects, Vol 3., Jolley, R. L., et. al., eds, Ann Arbor Science Publishers, Ann Arbor, Michigan.
21. Blanck, C., 1979, "Trihalomethane Reduction in Operating Water Treatment Plants," JAWWA 71:525.
22. Noack, M. G., and R. L. Doerr, 1978, “Reactions of Chlorine, Chlorine Dioxide and Mixtures Thereof with Humic Acid: An Interim Report.,” in Water Chlorination: Environmental Impact and Health Effects, Vol. 2., (R. L. Jolley, et. al., editors), Ann Arbor Science. Ann Arbor, MI.
23. Henderson, J. E., G. R. Peyton, and W. H. Glaze, 1976, “A Convenient Liquid-Liquid Extraction Method for the Determination of Halomethanes in Water at the ppb Level,” in Identification and Analysis of Organic Pollutants in Water, edited by Keith, L. H., Ann Arbor Science, Ann Arbor, MI., 105.
24. Lykins, B. W., and M. H. Griese, June 1986, “Using Chlorine Dioxide for Trihalomethane Control,” JAWWA 78:6:88.
25. Lykins, B. W., and W. Koffskey, August 1985, “Products Identified at an Alternative Disinfection Pilot Plant,” 2nd International Symposium on Health Effects of Drinking Water Disinfectants and Disinfection Byproducts, Cincinnati, OH.
26. Andrews, R. et al.,“Chlorine Dioxide Trial as a Post Disinfectant in Wiarton, Ontario, Fourth Int.Symp.International Symposium on Chlorine Dioxide, February 15-16, Las Vegas, Nevada (2001).
27. Synan, J.F., 1979, “Chlorine Dioxide - An Effective Biocide for Recycled or Reused Water Systems,” Trans. Citrus Eng. Conf., 25:66.
28. Rav-Acha, Ch., and R. Blits, 1985, “The Different Reaction Mechanisms by Which Chlorine and Chlorine Dioxide React with Polycyclic Aromatic Hydrocarbons (PAH) in Water,” Water Research, 19(10):1273.
29. Standard Methods for the Examination of Water and Wastewater, APHA, AWWA and WEF, Washington, D.C. (20th Ed. l998).
30. Methods for the Determination of Inorganic Substances in Environmental Samples. USEPA. 1993. EPA/600/R-93/100.
31. USEPAMethod 300.1, Determination of Inorganic Anions in Drinking Water by Ion Chromatography, Revision 1.0. USEPA. 1997. EPA/600/R-98/118
论文搜索
月热点论文
论文投稿
很多时候您的文章总是无缘变成铅字。研究做到关键时,试验有了起色时,是不是想和同行探讨一下,工作中有了心得,您是不是很想与人分享,那么不要只是默默工作了,写下来吧!投稿时,请以附件形式发至 [email protected] ,请注明论文投稿。一旦采用,我们会为您增加100枚金币。








